Cụ thể, Công ty M/s Windlas Biotech Limited (India) trụ sở chính tầng trệt, số 83 lô L, đường số 2, khu dân cư Phú Mỹ, phường Phú Mỹ, Quận 7, Tp.Hồ Chí Minh đã sản xuất thuốc vi phạm chất lượng mức độ 3 theo quy định của pháp luật đối với thuốc Locobile-200, số giấy đăng ký lưu hành VN-21822-19, số lô WLD21003E, ngày sản xuất 04/02/2021, hạn dùng 03/02/2024.
Theo điểm b, khoản 3, Điều 57, Nghị định số 117/2020/NĐ-CP ngày 28/9/2020 của Chính phủ quy định xử phạt vi phạm hành chính trong lĩnh vực y tế, phạt tiền 50 triệu đồng đối với doanh nghiệp về hành vi trên.
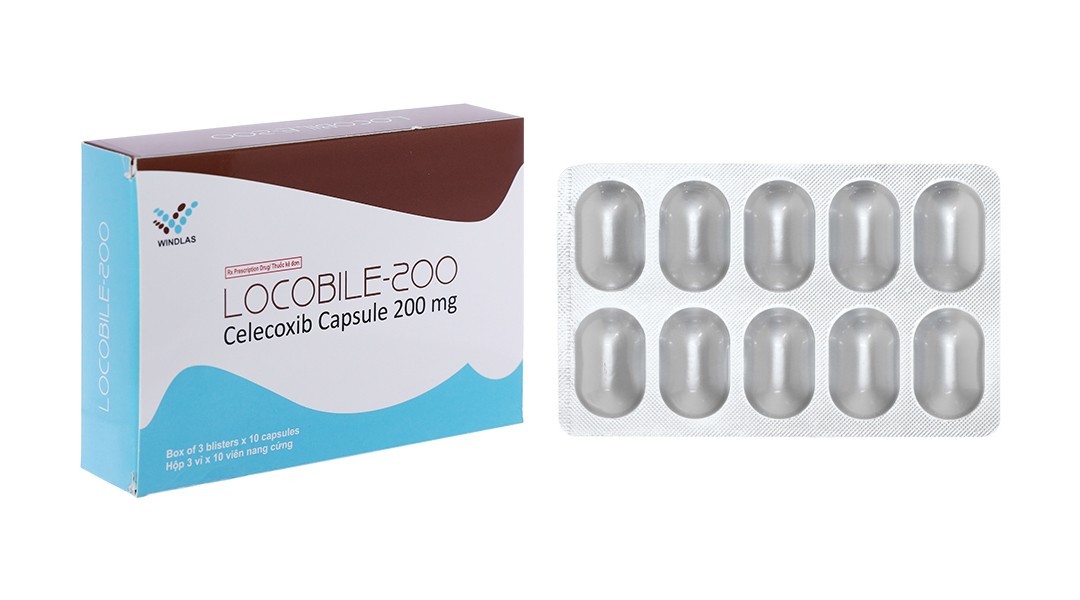
Đồng thời, giao cho công ty TNHH Dược phẩm Á Mỹ là cơ sở nhập khẩu lô thuốc Locobile-200 (số giấy đăng ký lưu hành VN-21822-19, số lô WLD21003E, ngày sản xuất 04/02/2021, hạn dùng 03/02/2024) tiến hành thu hồi toàn bộ số thuốc vi phạm chất lượng và báo cáo kết quả thực hiện về Cục Quản lý Dược theo yêu cầu tại Công văn số 2205/QLD-CL ngày 09/3/2023 của Cục Quản lý Dược.
Được biết, Locobile 200 được chỉ định để giảm đau và điều trị triệu chứng trong các bệnh lý: Thoái hóa khớp; viêm khớp dạng thấp; viêm cột sống dính khớp; các cơn đau cấp tính; đau bụng kinh (thống kinh).
Thạch Thảo